神取教授らの総説がChemical Reviews誌に掲載されました
Research
研究・産学官連携
2018年3月 8日掲載
神取教授らの総説がChemical Reviews誌に掲載
能動輸送のパナマ運河モデルと光駆動ナトリウムポンプ
大学院工学研究科 生命・応用化学専攻およびオプトバイオテクノロジー研究センターの神取秀樹教授・センター長、井上圭一准教授、角田 聡客員准教授による光駆動ナトリウムポンプに関する総説が、米国化学会のChemical Reviews誌に掲載されました。本誌は化学総説の最高峰として知られており、インパクトファクターも47.928とNature誌やScience誌を上回っています。本誌は招待執筆のみで構成され、多くの化学者にとって「一生のうちに一度は執筆したい」という憧れの存在です。神取教授は2014年にロドプシンの総説[1]を本誌に発表しており、二度目の執筆となる今回は、神取研究室の看板である光駆動ナトリウムポンプが対象となりました。
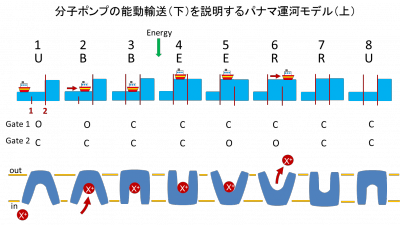
■ 分子ポンプの能動輸送とパナマ運河モデル
ヒトからバクテリアまで、細胞内にはカリウムイオンが、細胞外にはナトリウムイオンが多く、このようなイオンの濃度差が我々の生命を支えています。この濃度差をつくりだすのが分子ポンプと呼ばれる膜タンパク質であり、系のエントロピーを減少させるため、外部からのエネルギー入力が必要になります。濃度勾配に逆らったイオンの輸送を「能動輸送」と呼びますが、図下に示すようなX+イオンの上向き能動輸送は、図上のような「パナマ運河モデル」でよく説明されます。パナマ運河では、水位の高いところに船を運ぶため、2つのゲートとエネルギー入力による水位上昇を連動しています。図に示す通り、分子ポンプの8つの構造はパナマ運河の8つの状態と完全に対応しています。実際の分子ポンプはもっと複雑ですが、能動輸送のしくみはパナマ運河モデルにより見事に描くことができるのです。このような考え方は古くから知られていましたが、教科書などで厳密に記述した例はあまりなく、本総説の導入部で詳しく説明されています。
それは状態3と4の間のエネルギー入力の時点で船が入っていること(分子ポンプではイオンが結合していること)です。水位を上げたときに船が入っていなければエネルギーを使っても無駄な仕事になってしまうので、当然なことです。実際に、これまでに知られているほとんどすべての分子ポンプにおいて、イオンを結合している状態でエネルギー入力が起こっています。
■ 光駆動ナトリウムポンプの発見と研究の進展により明らかになった不思議なメカニズム
光のエネルギーを使ってイオンを一方向に能動輸送する光駆動イオンポンプとしては、プロトンポンプとクロライドポンプが40年以上前から知られていました。これらのポンプの場合も、光吸収というエネルギー入力が起こる前に、輸送されるプロトンやクロライドイオンはタンパク質内部に結合していますので、その点、パナマ運河モデルに従う分子ポンプと言うことができます。
一方、神取グループでは自然界に存在しないと信じられてきた光駆動ナトリウムポンプを2013年に発見しました[2]。さらに東大との共同研究によりこのタンパク質の立体構造を決定し、輸送モデルを提唱することができました[3]。またイオンの選択性を決める部位を突き止め、自然界に存在しないカリウムポンプ[3]やセシウムポンプ[4]を創成することにも成功しています。このように光駆動ナトリウムポンプ研究は神取研の看板として世界に鳴り響いており、このことがChemical Reviews誌から神取教授への二度目の執筆依頼へとつながりました。
神取教授によれば、光駆動ナトリウムポンプのいちばんの面白さは、能動輸送の特殊性にあるとのことです。研究チームは最初の論文で、ナトリウムイオンは内部ではなく出口側表面に結合することを分光実験により明らかにしていましたが、結合部位を欠損させてもポンプの機能は保たれていたのです[2]。この事実は、光駆動ナトリウムポンプがパナマ運河モデルに従わないことを示唆していました。その後、神取グループでは徹底的にこのタンパク質の性質を調べた結果、光駆動ナトリウムポンプが標準的なパナマ運河モデルに従わないことが明らかになりました。この分子ポンプは、船が入っていない状態でエネルギーを入力しても、船を運ぶことができるという不思議な輸送メカニズムを持つことがわかったのです。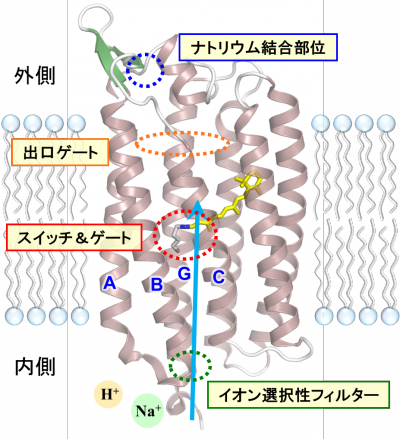
本総説では、パナマ運河モデルに従わない光駆動ナトリウムポンプに対して、修正パナマ運河モデルとも言うべきモデルを提案しています。光のエネルギーを巧みにタンパク質内部に貯め込むことで、ナトリウムイオンが拡散により入って来るまで待つことができるのです。このためには、パナマ運河モデルに必須の2つのゲートが正しく作動することが重要であり、このタンパク質はそのようにはたらいていることがわかってきました(図)。本総説のタイトルにある「新しい概念」とは、イオンを結合していなくても輸送できるメカニズムを指しています。
光駆動ナトリウムポンプは脳機能解明に大きな期待をされている新技術「光遺伝学(オプトジェネティクス)」のツールとしても有望であり、基礎から応用までの研究のさらなる発展が期待されます。
※今回の研究は、概算要求事業「光といのち」研究の世界拠点形成、日本学術振興会(JSPS)の科研費補助金、科学技術振興機構(JST)のCREST研究およびさきがけ研究の支援により実施されました。
"Light-Driven Sodium-Pumping Rhodopsin: A New Concept of Active Transport"
Hideki Kandori, Keiichi Inoue, Satoshi P. Tsunoda
Chem. Rev. (2018).
DOI:10.1021/acs.chemrev.7b00548
<参考文献>
[1] O. P. Ernst, D. T. Lodowski, M. Elstner, P. Hegemann, L. S. Brown, H. Kandori, "Microbial and animal rhodopsins: Structures, functions, and molecular mechanisms", Chem. Rev. 114, 126-163 (2014).
https://pubs.acs.org/doi/10.1021/cr4003769
[2] K. Inoue, H. Ono, R. Abe-Yoshizumi, S. Yoshizawa, H. Ito, K. Kogure, H. Kandori, "A light-driven sodium ion pump in marine bacteria", Nat. Commun. 4, 1678 (2013).
[3] H. E. Kato, K. Inoue, R. Abe-Yoshizumi, Y. Kato, H. Ono, M. Konno, S. Hososhima, T. Ishizuka, M. R. Hoque, H. Kunitomo, J. Ito, S. Yoshizawa, K. Yamashita, M. Takemoto, T. Nishizawa, R. Taniguchi, K. Kogure, A. D. Maturana, Y. Iino, H. Yawo, R. Ishitani, H. Kandori, O. Nureki, "Structural basis for Na+ transport mechanism by a light-driven Na+ pump", Nature 521, 48-53 (2015).
[4] M. Konno, Y. Kato, H. E. Kato, K. Inoue, O. Nureki, H. Kandori, "Mutant of a light-driven sodium ion pump can transport cesium ions", J. Phys. Chem. Lett. 7, 51-55 (2016).
メイちゃんの弟の名前が決定しました! 柴田研究室の研究成果がOrganic Chemistry Frontiers 誌のFront Cover Pictureで紹介されました
この情報は研究支援課が提供しています。