次世代光遺伝学を支える光駆動ナトリウムポンプの分子機構を解明 ~脳神経研究に貢献する光制御ツール開発へ前進~
News&Topics
カテゴリ:プレスリリース|2026年2月26日掲載
発表のポイント
○ 海洋性細菌由来の光駆動ナトリウムポンプにおける、ナトリウムイオン(Na+)輸送中の分子構造変化を時間分解赤外分光法で解明
○ Na+輸送の鍵となる反応中間体において、アスパラギン残基とNa+の動的相互作用を明らかに
○ アスパラギン酸残基近傍でのNa+の脱着が、輸送を助ける補助的機構であることを示唆
概要
名古屋工業大学生命・応用化学類の古谷祐詞准教授らは、細胞内イオン環境に左右されにくい新たな神経抑制法として期待される光駆動ナトリウムポンプ「KR2」について、時間分解赤外分光法を用いて光反応に伴う分子の動きを振動として捉え、Na+輸送の分子構造変化を解明しました。
光駆動ナトリウムポンプ「KR2」は、2013年に神取秀樹教授(現 特別教授)を中心とする研究グループが海洋性細菌から世界で初めて発見した、光を受けて細胞外へNa+をくみ出すタンパク質です。しかし、その詳細な分子機構は未解明でした。
今回の研究では、Na+輸送の分子機構を詳しく解析し、112番目のアスパラギン残基がNa+結合に重要な役割を果たすことを明らかにしました。さらに、輸送に関与するO中間体が2つの状態(O1とO2)を経て構造変化することを示しました。また、輸送されるNa+とは別に、細胞外側の102番目のアスパラギン酸残基近傍で脱着するNa+が放出過程を助ける新機構も提案しました。
本成果は、神経細胞の興奮を光で抑える光遺伝学ツールの高度化や、カリウムポンプ型変異体の高性能化につながる基礎的知見であり、脳機能の解明や神経疾患研究への応用が期待されます。
本研究成果は、2026年2月26日に米国生化学・分子生物学会のオープンアクセス誌Journal of Biological Chemistryのオンライン速報版に掲載されました。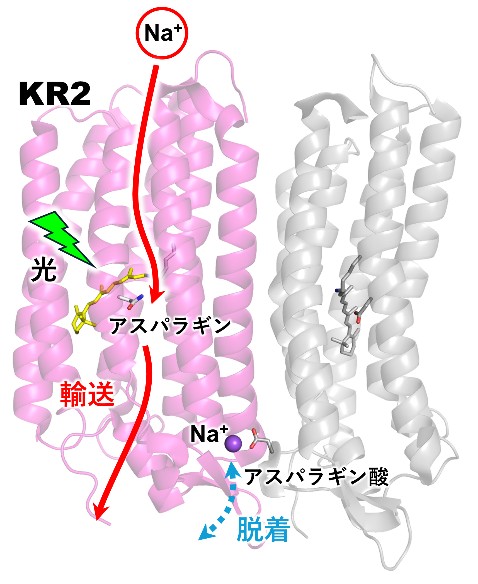
▶詳細(プレスリリース本文)はこちら
論文情報
論文名:Mechanistic insights into Na⁺ pumping by KR2: distinct roles of Asp102 and Asn112 coupled with retinal distortion in two O intermediates
著者名:Sahoko Tomida, Rei Abe-Yoshizumi, Akimori Wada, Hideki Kandori and Yuji Furutani* *責任著者
掲載雑誌名:Journal of Biological Chemistry
DOI:10.1016/j.jbc.2026.111313
URL:https://www.jbc.org/article/S0021-9258(26)00183-3/fulltext
用語解説
(*1)光遺伝学(オプトジェネティクス)
光に反応するタンパク質を神経細胞などに導入し、光を照射することで細胞の活動を人為的に制御する技術。光感受性タンパク質としては、微生物由来のロドプシンが広く用いられる。これらは光を受けるとイオンを細胞内外へ移動させる働きを持ち、神経細胞の興奮や抑制を瞬時に操作できる。電気刺激と比べて高い時間分解能と細胞選択性を兼ね備えていることが特徴である。現在では、脳回路の機能解明や行動研究に不可欠な基礎研究手法として発展しており、将来的には神経疾患の治療法への応用も期待されている。
研究支援
本研究は以下の助成により実施されました:
• 日本学術振興会 科学研究費補助金(JP24H00451)
• 文部科学省「大学の研究力強化促進事業(CURE)」(JPMXP1323015482)
• 科学技術振興機構CREST「細胞操作」領域(JPMJCR25B5)
• 大幸財団、立松財団
お問い合わせ先
(研究に関すること)
名古屋工業大学 生命・応用化学類
准教授 古谷 祐詞
TEL:052-735-5127
E-mail:furutani.yuji[at]nitech.ac.jp
(広報に関すること)
名古屋工業大学 企画広報課
TEL:052-735-5647
E-mail:pr[at]adm.nitech.ac.jp
*それぞれ[at]を@に置換してください。
固定化処理プラントで回収SF6ガスから高純度蛍石生成に成功― 年間2トン処理・温室効果ガス削減を実現し実用化へ ― 薬になりにくい―天然物創薬の限界を突破する合成法確立 赤痢アメーバ症はじめさまざまな疾患治療薬への展開に期待

