「薬剤蛋白質を充填可能な蛋白質カプセル」のドラッグデリバリー担体への利用―抗体の表面修飾により、標的細胞のみへの薬剤蛋白質の導入に成功―
News&Topics
カテゴリ:プレスリリース|2024年8月30日掲載
発表のポイント
〇 200分子以上の薬剤蛋白質をカプセル内部に充填可能な、両親媒性蛋白質から組み上げられる蛋白質カプセルの作成に、世界で初めて成功
〇 抗体蛋白質の表面修飾により、粒径100nmを超えるこの蛋白質カプセルを、狙った細胞の細胞内部に選択的に送り込むことが可能
〇 薬剤として機能する蛋白質を予めカプセルの内部に充填させておくことで、狙った細胞のみに選択的に送達し、細胞内部でその薬剤を働かせることに成功
概要
名古屋工業大学工学専攻生命・応用化学系プログラム(研究当時)の高橋 孝介氏、生命・応用化学科の細田 琉貴氏、生命・応用化学類の水野 稔久准教授らのグループは、名古屋市立大学、東北大学、北九州市立大学との共同研究により、薬剤蛋白質(注1)を標的とする哺乳類細胞に選択的に送り込むことが可能な、抗体を表面修飾した蛋白質カプセルの構築に成功しました(図1)。ここで用いた蛋白質カプセルは、本研究グループによりオリジナル設計された、特殊な両親媒性が付与されたツーヘリックスバンドル蛋白質(注2)から構築され、この蛋白質カプセルの構築原理についても、世界で初めて明らかとしたものです。この蛋白質カプセルは直径100 nmを超える粒径を持ちつつも十分な構造的安定を保ち、1カプセルあたり200分子以上の薬剤蛋白質を、変性失活させることなくその内部に安定に充填可能です。またこのカプセル表面に、標的細胞(例えばガン細胞)に特異的な抗体(IgG抗体やVHH抗体)を修飾することで、狙った細胞のみに取り込ませる機能が付与可能であり、細胞内部で薬剤蛋白質をリリースすることで、その薬効を発現させることにも成功しました。
本研究成果は2024年8月1日にRSC Pharmaceuticsに掲載されました。
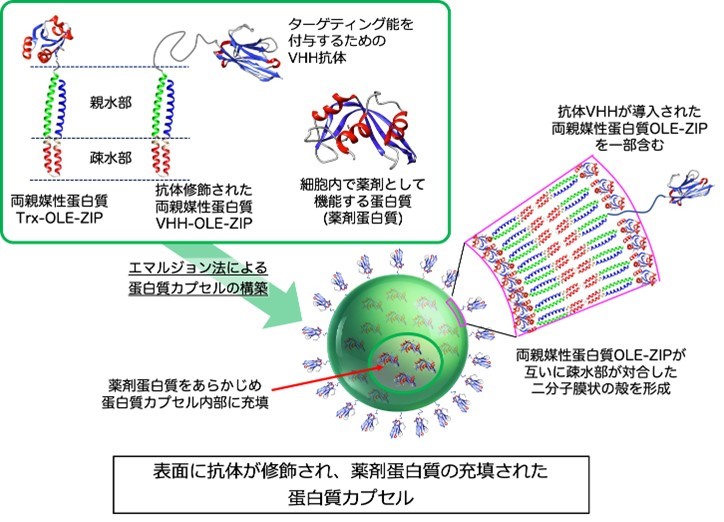
図1 両親媒性蛋白質(注3)から構築される、抗体が表面修飾された蛋白質カプセルの模式図
研究の背景
近年、従来ある低分子量の有機化合物を中心とした医薬品に加え、蛋白質や核酸などの生体高分子を用いるバイオ医薬品の利用が進んでいます。キナーゼなどをターゲットにした分子標的薬の登場により、低分子医薬品についても副作用を低減する取り組みはなされていますが、元々副作用の起こりにくいバイオ医薬品のさらなる利用拡大が望まれています。
現在利用されているバイオ医薬品の1つに抗体医薬品がありますが、細胞内へはほとんど取り込まれないため、基本的には細胞外表面で機能させるものからしか創薬はなされていません。この自発的には細胞内に取り込まれない性質により副作用が起こりにくくなっていますが、逆にいえば細胞内で生命活動に直接関与している大多数の生体分子をターゲットとした創薬はできておらず、バイオ医薬品が対象とする創薬シーズを制限する原因となっています。この課題の解決に向け、現在、抗体も含めた蛋白質ベースのバイオ医薬品を、標的細胞に効率よく導入可能とする技術開発への取組みが世界的に行われています。
研究の内容・成果
天然には内部空孔を保持した蛋白質会合体(以下、蛋白質カプセル)がいくつか知られており、近年ではAlphaFold 3などの構造予測プログラムを用いた設計開発も進められています。また蛋白質カプセルは、薬剤蛋白質に対するドラッグデリバリー担体としての利用にも注目が集まっています。大半の蛋白質カプセルは、100分子を超えるサブユニット蛋白質から組み上げられて構築されますが、内部空孔サイズが10 nmを超えるものは少なく、多数の薬剤蛋白質を内部に充填可能な100 nmを超える内部空孔を持った蛋白質カプセルを人工的に設計・構築することは、仮に構造予測プログラムを用いたとしても難しいのが現状です。
そこで本研究では見方を変えて、2本のαヘリックスが束なる2ヘリックスバンドル蛋白質の片側表面を疎水性、もう片側を親水性とした両親媒性蛋白質を新たにデザインし、エマルジョン法を用いてリン脂質の形成するリポソームのように集合化させることで、ドラッグデリバリー担体としての要件を満たす、蛋白質カプセルの構築が可能ではないかと着想しました。なお、ここで用いた両親媒性蛋白質は、油を絞ることが可能な植物種子に広く分布する両親媒性蛋白質オレオシンの一部の蛋白質配列と、天然にあるDNA結合蛋白質の構造モチーフとしても知られるコイルドコイルの蛋白質配列を組み合わせることで、独自に設計を行いました。
このタンパク質は直径100 nmを超える粒径を持ちつつも十分な構造的安定を保ち、凍結乾燥などの乾燥操作後にもカプセル形態は維持されました。またこの蛋白質カプセル調製時に、内包させたい薬剤蛋白質を予め添加することで、1カプセルあたり200分子以上を、カプセル内部に変性失活させることなく充填が可能であり、この状態でもカプセル形態は維持されました。一方でこのカプセル単独では哺乳類細胞内への取り込みは見られませんでしたが、カプセル表面に標的細胞(例えばガン細胞)に特異的な抗体分子を修飾することで、受容体を媒介したエンドサトシスにより標的細胞への取り込みが誘導されました(図2)。その結果、カプセル内部に予め充填していた薬剤蛋白質を、狙った細胞の細胞質内に選択的に送り込み、その薬効の発現に成功しました(当初目的となる薬剤蛋白質のドラッグデリバリー担体として十分に機能する、蛋白質カプセルの開発に成功)。なお、これまでに抗体を修飾したウイルスキャプシド蛋白質を用い、核酸の細胞種選択的な送達に成功した報告例はありますが、本研究成果は、薬剤蛋白質を充填した蛋白質カプセルを抗体と複合化することで、薬剤蛋白質に対する細胞種選択的なキャリアとして利用することに成功した世界初の例でもあります。
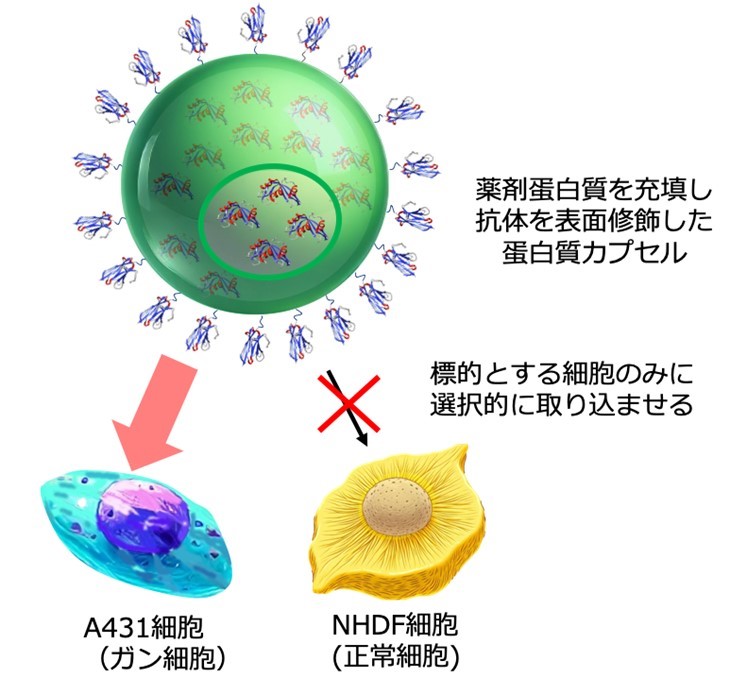
図2 抗体修飾した蛋白質カプセルを用いた細胞種選択的な薬剤蛋白質の送達
社会的な意義
近年の新型コロナウイルスの世界的な猛威への対策として、バイオ医薬品の1つであるm-RNAワクチンが大きな注目を集めましたが、生体高分子を薬として利用する医薬品開発は、今後より一層拡大すると予想されます。しかしこれらの利用拡大には、バイオ医薬品の持つ欠点や限界点を補う技術開発の発展も必須であり、今回の抗体修飾された蛋白質カプセル型のドラッグデリバリー担体は、膜透過性の低さに対する問題解決だけでなく、血中投与時に危惧される免疫によるクリアランスの回避も期待できます。また非常に大きな内部空孔を持った蛋白質カプセルであるため、より巨大な薬理活性の見込まれる蛋白質複合体、蛋白質-核酸複合体などの送達も期待され、単分子ベースの生体高分子を元にした医薬品開発ではなく、より複雑な蛋白質複合体の医薬品利用を可能とする研究開発への新たな示唆を与える研究成果となります。
今後の展望
本研究で開発した蛋白質カプセルの抗体部分は、標的細胞ごとに置き換えることができ、さらにカプセル内部には様々な薬剤蛋白質の充填が可能です。したがって、様々な哺乳類細胞に対して選択性を持たせた蛋白質カプセル型のドラッグデリバリーキャリア開発の発展が期待されます。本研究グループでは前臨床段階の検討として、実験動物を利用した有効性の検証にも今後取り組んでいく予定です。
本研究は、公益財団法人池谷科学技術振興財団、公益財団法人泉科学技術振興財団のサポートにより、なされた成果となります。
用語解説
(注1)薬剤蛋白質:ここで該当する薬剤蛋白質とは、細胞内に導入された時に薬効の期待される蛋白質全般を想定しており、例えば、核酸合成酵素、核酸結合蛋白質、シグナル伝達蛋白質などへの結合活性を持った蛋白質なども考えられる。本研究論文内では、デモンストレーションとしてRNAの加水分解酵素や相同組み換え酵素を用いている。
(注2)ツーヘリックスバンドル蛋白質:2本のαヘリックスがリンカーペプチドを介して繋がり、安定に2量体構造を形成する蛋白質。全体として、棒状の立体構造をとる。
(注3)両親媒性蛋白質:ここでは、棒状の立体構造を持つツーヘリックスバンドル蛋白質の片側表面に疎水性、もう片側表面に親水性を持たせた蛋白質をさす。この分子構造内に疎水部、親水部が偏って配置されることで、これらの蛋白質間で働く相互作用をコントロールし、これらの間の相互作用により形成される蛋白質カプセルは、水中で安定化される。
論文情報
論文名:Target-selective cytosolic delivery of cargo proteins using the VHH-presented OLE-ZIP capsules
著者名:Kousuke Takahashi, Yasumichi Inoue, Shigeaki Hida, Ryuki Hosoda, Naoki Umezawa, Isamu Akiba, Mitsuo Umetsu, Toshihisa Mizuno*
掲載雑誌名:RSC Pharmaceutics
公表日:2024年8月1日
DOI:10.1039/D4PM00069B
URL:https://pubs.rsc.org/en/Content/ArticleLanding/2024/PM/D4PM00069B
お問い合わせ先
研究に関すること
名古屋工業大学 生命・応用化学類
准教授 水野 稔久
TEL: 052-735-5237
E-mail: toshitcm[at]nitech.ac.jp
広報に関すること
名古屋工業大学 企画広報課
TEL: 052-735-5647
Email: pr[at]adm.nitech.ac.jp
*[at]を@に置換してください。
電子材料技術の鍵となる新奇ペロブスカイト強誘電体を発見 ~分子レベルの積木細工で、未踏物質の合成に成功~ 実用的な高エネルギー密度のコバルト・ニッケルフリー電池材料を開発―ナノ構造を高度に制御したリチウムマンガン酸化物材料の合成に成功―

